Partikelkontamination
Als Partikelkontaminationen bezeichnet man das Vorliegen von Partikeln in einer Infusionslösung, welche unbeabsichtigt von außen eingetragen wurden. Die Partikelgrößen sind unterschiedlich, man grenzt die mit dem bloßen Auge sichtbaren Partikel der Größe ≥ 50 μm von den nicht sichtbaren Partikeln im Bereich von 2 - 50 μm ab. Vor allem der Nachweis von nicht mit dem bloßen Auge erkennbaren Partikeln erfordert spezifische analytische Tests.
Wussten Sie schon?
Ursachen
Es sind mehrere Ursachen für Partikelkontaminationen in intravenösen Lösungen bekannt, da Medikamente in unterschiedlichen Arten von Behältern verfügbar sind (z.B. Glasfläschchen, Ampullen, vorbefüllte Behälter und vorgemischte Lösungen) und in Handhabung und Anwendung sehr unterschiedlich sein können. Dementsprechend kann es zu verschiedenen Arten von Partikelkontaminationen kommen.
Glas
Glasampullen stellen ein besonders hohes Risiko für Partikelkontaminationen dar, weil beim Öffnen der Ampulle winzige Glassplitter in die Ampulle gelangen können.6 Wenn für das Aufziehen des Inhalts einer Glasampulle eine Kanüle (z. B. 18G) verwendet wird, können winzige Glaspartikel mit in die Spritze aufgezogen werden und dann in den Körper des Patienten gelangen.
Dieses Risiko bleibt auch dann bestehen, wenn Arzneimittel routinemäßig über den Injektionsport der Venenverweilkanüle verabreicht werden, denn dieser Port enthält keinen Partikelfilter.6,7
Kontamination durch Kunststoff
Eine Kontamination durch Kunststoff entsteht meist durch:
- Partikel, die aus dem Rohmaterial des Behälters stammen
- Partikel, die im Injektionsport bei Verwendung scharfer Gegenstände abgeschabt werden
Gummipartikel
Beim Einstechen einer Kanüle durch den Stopfen einer Arzneiampulle oder eines Infusionsbehälters kann es zum Ausstanzen eines Stopfenfragments kommen. Dieses Fragment kann dann in die Medikation/Infusionslösung gelangen. Wenn das Fragment sehr klein oder verdeckt ist (z. B. durch das Etikett, einen gleichfarbigen Hintergrund oder durch die Färbung der Ampulle), bleibt die Kontamination möglicherweise unbemerkt. Der Gummipartikel wird dann eventuell in eine Spritze gezogen und einem Patienten injiziert.8
Nicht gelöste Feststoffe
Auch nicht gelöste Feststoffe in Arzneimitteln oder parenteralen Lösungen können der Ursprung von Partikelkontaminationen sein.3,9
Folgen
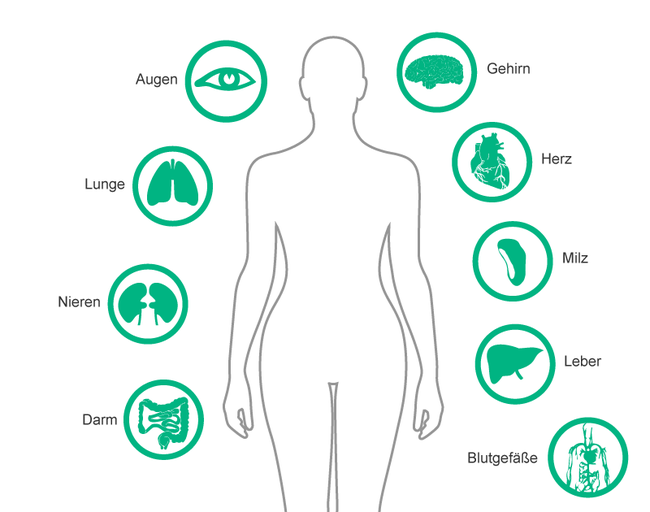
Abb. 1: Übersicht der Körperteile und Organe des menschlichen Körpers, die hauptsächlich durch Partikelkontamination betroffen sind.
Alle Formen von Partikeln, die im intraluminalen Kompartment vorliegen und nicht durch einen Filter zurückgehalten werden, gelangen direkt in den menschlichen Körper. Diese Kunststoff-, Glas- oder Gummipartikel können unerwünschte Effekte haben, insbesondere bereits erkrankte Menschen können davon betroffen sein.
Bei Patienten können schon Partikel, die nur 1,5 μm groß sind, zur Verlegung von Gefäßen führen, während dies bei Gesunden erst für Partikel ab einer Größe von 6 μm beschrieben wurde.3,4,5
Generell wurden als Folgen Organschädigungen von Lunge, Niere, Leber und Milz beschrieben.1,9 Schwerkranke Patienten waren jedoch besonders stark betroffen.4,5,10,11 Besonders empfindlich reagierten Patienten mit vorbestehenden Organschädigungen, da die Partikel die bereits beeinträchtigte Mikrozirkulation noch weiter verschlechterten.4,5
Ein weiteres klinisches Problem, das durch Glaspartikel aus Glasampullen verursacht werden kann, ist die Phlebitis.3,4,12 Eine Phlebitis manifestiert sich als lokale Überwärmung, Schmerzen und Rötung am Verabreichungsort der parenteralen Medikation.13
Präventionsstrategien
Die Prävention von Partikelkontaminationen an deren Entstehung erfordert eine breit angelegte Strategie:
- die Verwendung von Qualitätsprodukten, um Partikelbildung zu vermeiden (z. B. Verschlussstopfen)
- der Einsatz von Produkten mit niedrigem intrinsischem Partikelgehalt (z. B. Kunststoff- statt Glasampullen)
- die Prävention von Arzneimittelinkompatibilitäten
Partikelkontaminationen lassen sich vermindern, wenn Inline-Filter und Filterkanülen zum Aufziehen der Arzneimittel aus Glasampullen verwendet werden, bevor die Applikation erfolgt.
Inline-Filter:
- reduzieren Partikelkontaminationen
- vermindern mikrobiologische Kontaminationen
- scheiden Luft aus Infusionslösungen ab
Falls es zu einer Partikelkontamination kommt, bieten Inline-Filter einen wichtigen Sicherheitsvorteil.
Außerdem bieten Inline-Filter folgende Funktionen:
- Frühwarnsystem
- Optische Kontrolle der Infusionslösung
- Stoppen die Infusion, wenn der Filter blockiert ist
Die Filtration von Infusionslösungen ist jedoch keine gängige Praxis.
Inline- Filter in der Infusionsleitung sollten patientennah positioniert werden. Sie werden entsprechend ihrer Porengröße für folgende Lösungen empfohlen:
- 0,2 µm-Filter: Lösungen, die keine Fette enthalten14
- 1,2 µm-Filter: Lipidlösungen und Zubereitungen für die totale parenterale Ernährung14
- Die ISO-Norm 8536-4 (für Infusionssets) empfiehlt die Filterung zum Schutz des Patienten. Generell sollte der Flüssigkeitsfilter eine nominale Porengröße von 15 μm haben (ISO 8536-4).
Die British Pharmaceutical Nutrition Group (BPNG) erläutert in einer Leitlinie, wie die Kontamination mit unlöslichen Partikeln vermieden werden kann.14,15
- Lösungen, die aus Glasampullen oder -fläschchen in ein parenterales Ernährungsgemisch eingebracht werden, sollten durch einen Filter mit einer maximalen Porengröße von 5 μm aufgezogen werden. Filterkanülen und Dispensernadeln (Spikes) mit Partikelfilter vermindern das Risiko der Einschleppung von Glaspartikeln in den Patienten (Abb. 3).
- Bei der Versorgung von Patienten, die eine intensive oder langfristige parenterale Therapie brauchen, insbesondere Patienten mit Immunschwäche, Neugeborene und Kinder sowie Patienten, die zu Hause parenteral ernährt werden, sollten geeignete Filter verwendet werden.
Produktempfehlung zur Risikoprävention
Literaturangaben
1 Werner BP, Winter G. (2015) Particle contamination of parenteralia and in-line filtration of proteinaceous drugs. Int J Pharm;496(2):250-67
2 Doessegger L, Mahler HC, Szczesny P, Rockstroh H, Kallmeyer G, Langenkamp A, Herrmann J, Famulare J. (2012) The potential clinical relevance of visible particles in parenteral drugs. J Pharm Sci; 101(8): 2635-44
3 Ortolani GA, Russell RL, Angelbeck JA, Schaffer J, Wenz B. (2004) Contamination control in nursing with filtration. Part 1: filters applied to intravenous fluids and point-of-use hospital water. J Infus Nurs; 27(2): 89-103
4 Anonymus [No authors listed]. (2004) Risks due to particles in infusion therapy--experts promote use of infusion filters. Krankenpfl J. 2004; 42(3-4): 97
5 Lehr HA, Brunner J, Rangoonwala R, Kirkpatrick CJ. (2002) Particulate matter contamination of intravenous antibiotics aggravates loss of functional capillary density in postischemic striated muscle. Am J Respir Crit Care Med; 165:514-520
6 Lee KR, Chae YJ, Cho SE, Chung SJ. (2011) A strategy for reducing particulate contamination on opening glass ampoules and development of evaluation methods for its application. Drug Dev Ind Pharm; 37(12): 1394-401
7 Lye ST, Hwang NC. (2003) Glass particle contamination: is it here to stay? Anaesthesia; 58(1): 93-4
8 Roth JV. (2007) How to enter a medication vial without coring. Anesth Analg; 104(6): 1615
9 Boehne M, Jack T, Köditz H, Seidemann K, Schmidt F, Abura M, Bertram H, Sasse M. (2013) In-line filtration minimizes organ dysfunction: new aspects from a prospective, randomized, controlled trial. BMC Pediatr; 13 : 21
10 Jack T, Boehne M, Brent BE, Hoy L, Köditz H, Wessel A, Sasse M. (2012) In-line filtration reduces severe complications and length of stay on pediatric intensive care unit: a prospective, randomized, controlled trial. Intensive Care Med; 38(6): 1008-1
11 Oie S, Kamiya A. (2005) Particulate and microbial contamination in in-use admixed parenteral nutrition solutions. Biol Pharm Bull; 28(12): 2268-70
12 Yorioka K, Oie S, Oomaki M, Imamura A, Kamiya A. (2006) Particulate and microbial contamination in in-use admixed intravenous infusions. Biol Pharm Bull;29(11):2321-3,
http://www.ncbi.nlm.nih.gov/pubmed/17077539 (Zugriff 06.2021)
13 Nassaji-Zavareh M, Ghorbani R. Peripheral intravenous catheter-related phlebitis and related risk factors. Singapore Med J. 2007 Aug;48(8):733-6
14 Ball PA. (2003) Intravenous in-line filters: filtering the evidence. Curr Opin Clin Nutr Metab Care; 6(3): 319-25
15 Bethune K Allwood M, Grainger C, Wormleighton C; British Pharmaceutical Nutrition Group Working Party. (2001) Use of filters during the preparation and administration of parenteral nutrition: position paper and guidelines prepared by a British pharmaceutical nutrition group working party. Nutrition;17(5):403-8











